Les applications en aval jouent un rôle important dans la chaîne de valeur de l'hydrogène
World Platinum Investment Council | En raison de sa polyvalence en tant que carburant, matière première chimique et vecteur énergétique, l'hydrogène est essentiel à la transition énergétique, en particulier lorsqu’il est produit sous forme d’hydrogène vert à partir de sources renouvelables. Les métaux du groupe du platine (PGM) sont essentiels pour permettre l’utilisation de l’hydrogène (vert) afin d’atteindre les objectifs de décarbonisation.
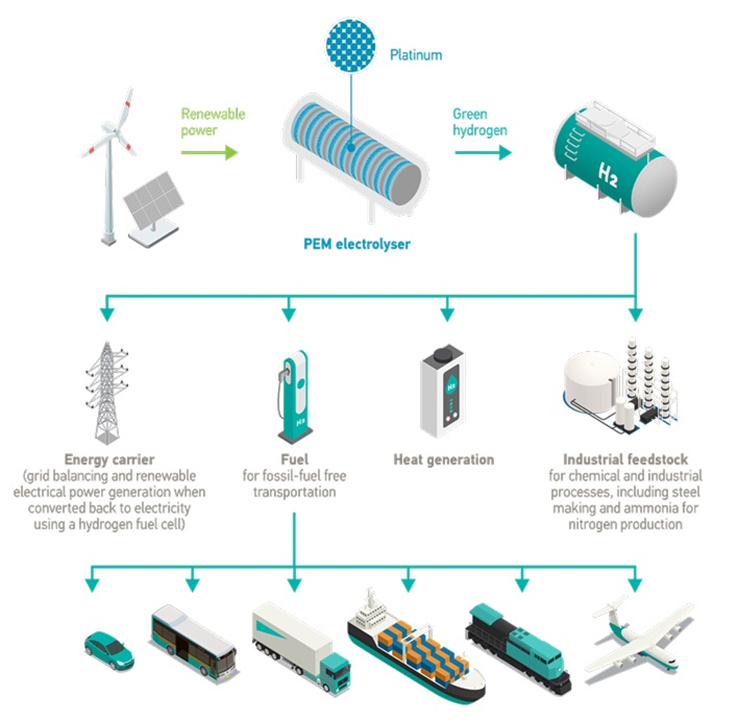
Les métaux du groupe du platine (PGM) sont utilisés tout au long de la chaîne de valeur de l'hydrogène dans diverses applications. L'accent est souvent mis sur l'utilisation de catalyseurs à base de PGM dans la technologie des membranes à échange de protons (PEM), tant en amont (électrolyseurs permettant de produire de l'hydrogène par dissociation de l'eau en oxygène et en hydrogène) qu'en aval (piles à combustible à hydrogène pour la production d'électricité).
Parmi cette demande, les piles à combustible utilisées tant dans le secteur de la mobilité (transports terrestres, maritimes et aériens) que dans les applications stationnaires constituent le segment le plus important de la demande prévue de platine liée à l'hydrogène, qui devrait dépasser les 600 000 onces d'ici 2030.
Cependant, les applications en aval qui nécessitent des métaux du groupe du platine (PGM) jouent également un rôle important dans le développement du marché et la mise en place d'un commerce mondial de l'hydrogène vert. Applications en aval Les utilisations des métaux du groupe du platine (PGM) en aval de la chaîne de valeur de l'hydrogène comprennent la purification de l'hydrogène issu des électrolyseurs, le craquage de l'ammoniac et le chargement de l'hydrogène dans un vecteur organique liquide (LOHC) à des fins de transport et de stockage.
.png)
Les métaux du groupe du platine (PGM) sont de plus en plus utilisés pour produire des carburants synthétiques, tels que les carburants aériens durables (SAF). Lors de l'électrolyse, la séparation des gaz n'est pas nécessairement parfaite. Selon la technologie d'électrolyse utilisée, il existe un certain degré de « mélange » entre les deux gaz. Par conséquent, une purification s'avère nécessaire, et la séparation électrochimique est l'une des méthodes les plus couramment utilisées pour purifier l'hydrogène.
Ce phénomène se produit dans un purificateur d'hydrogène au palladium, où le processus de séparation est facilité par voie électrochimique grâce aux propriétés catalytiques des membranes recouvertes de palladium. À mesure que l'économie de l'hydrogène se développe, il sera nécessaire de transporter l'hydrogène à l'échelle nationale et mondiale afin de relier les sites de production à la demande finale émergente.
Si l'hydrogène présente une densité énergétique massique (énergie par kilogramme) supérieure à celle des carburants liquides classiques tels que l'essence, sa densité énergétique volumique est en revanche plus faible, ce qui le rend très léger et donc difficile à transporter sur de longues distances. Il est toutefois possible de transporter l'hydrogène sous forme de produits dérivés, comme l'ammoniac, ou à l'aide d'un LOHC.
Grâce à des densités énergétiques plus élevées par unité de volume, ces méthodes améliorent l'efficacité du transport. L'hydrogène transporté et stocké chimiquement sous forme d'ammoniac est libéré lors d'une réaction chimique appelée « craquage de l'ammoniac ». Le craquage de l'ammoniac en hydrogène et en azote nécessite un environnement à haute température et haute pression.
Pour réduire la température et la pression afin d'optimiser la consommation d'énergie, on utilise souvent un catalyseur à base de métaux du groupe du platine (PGM), généralement du ruthénium. Les LOHC absorbent et libèrent de l'hydrogène par le biais de réactions chimiques. Lorsque l'hydrogène est absorbé dans le support organique liquide, on utilise des catalyseurs d'hydrogénation à base de métaux du groupe du platine (PGM), notamment du platine.
Les LOHC peuvent ensuite être stockés et transportés à température et pression ambiantes, en utilisant les infrastructures existantes de distribution de carburant. Le platine est également utilisé comme catalyseur dans le processus de déshydrogénation qui libère l'hydrogène contenu dans les LOHC.
Également appelés « carburants synthétiques », les e-carburants sont des carburants à faible empreinte carbone ou neutres en carbone, obtenus en combinant du dioxyde de carbone issu de sources durables avec de l'hydrogène produit par électrolyse en présence d'un catalyseur à base de métaux du groupe du platine. Avec quelques modifications mineures, les e-carburants peuvent remplacer directement les carburants fossiles dans les moteurs à combustion interne.












-Logo_CMYK_1.jpg?width=1000&height=500&ext=.jpg)









.png?width=300&height=208&ext=.png)

_mi25-weblogo.png?ext=.png)

_1.png?ext=.png)

































_logo.png?ext=.png)

_mi25-weblogo.png?ext=.png)




